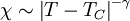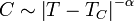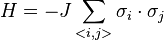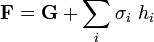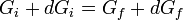Transizione di fase
In fisica e in chimica, una transizione di fase[1] (o passaggio di stato o cambiamento di stato) è la trasformazione di un sistema termodinamico da uno stato di aggregazione ad un altro.[2] La caratteristica distintiva di una transizione di fase è il brusco cambiamento di una o più proprietà fisiche, in particolare la capacità termica, alla minima variazione di variabili termodinamiche come la temperatura. Alcuni esempi di transizioni di fase sono:
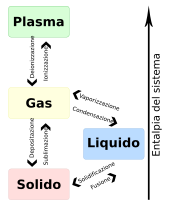
- Le transizioni tra le fasi solida, liquida, e aeriforme (ebollizione, fusione, sublimazione, ecc.)
- La transizione tra le fasi ferromagnetica e paramagnetica dei materiali magnetici al punto di Curie.
- La superconduttività in certi metalli sotto una temperatura critica.
- La condensazione quantistica dei liquidi bosonici come la condensazione di Bose-Einstein e la transizione del superfluido in elio liquido.
- La rottura delle simmetrie nelle leggi fisiche al raffreddarsi della temperatura dell'universo.
- Il folding delle proteine.
Le transizioni di fase avvengono quando l'energia libera di un sistema è non-analitica per alcuni valori delle variabili termodinamiche. Questa non-analiticità generalmente proviene da sistemi con un alto numero di particelle e non è presente in sistemi molto piccoli.
Indice |
[modifica] Classificazione delle transizioni di fase
[modifica] Classificazione di Ehrenfest
Il primo tentativo si classificare le transizioni di fase è dovuto a Paul Ehrenfest, che raggruppò le transizioni di fase in base ai gradi di non-analiticità coinvolti. Sebbene utile, la classificazione di Ehrenfest risulta difettosa, come si vedrà successivamente.
Sotto questo schema, le transizioni di fase erano classificate in due gruppi dalla più bassa derivata dell'energia libera di Gibbs (entalpia libera) che risultava discontinua al momento della transizione. La transizione di fase del primo ordine presenta una discontinuità nella derivata prima dell'energia libera, calcolata rispetto ad una variabile termodinamica. Le varie transizioni solido/liquido/gas sono classificate al primo ordine in quanto è la pressione, che è la derivata prima dell'energia libera rispetto al volume, a cambiare con discontinuità lungo la transizione.
Le transizioni di fase del secondo ordine hanno una discontinuità in una derivata seconda dell'energia libera. Queste includono la transizione alla fase ferromagnetica in materiali come il ferro, dove la magnetizzazione, che è la derivata prima dell'energia libera rispetto al campo magnetico applicato, cresce dallo zero con continuità non appena la temperatura è al si sotto di quella di Curie, mentre la suscettività magnetica, che è la derivata seconda dell'energia libera rispetto al campo, cambia con discontinuità. Nello schema di Ehrenfest, potrebbero esserci, in principio, transizioni di fase del terzo ordine, del quarto, e così via.
[modifica] Classificazione moderna delle transizioni di fase
Lo schema di Ehrenfest è un metodo di classificazione poco accurato, in quanto basato sulla teoria di campo medio: questa è inesatta in vicinanza della transizione di fase, poiché, come si vedrà, trascura le fluttuazioni. Per esempio, predice una discontinuità finita nella capacità termica alla transizione ferromagnetica, ovvero una transizione del "secondo ordine", secondo la definizione di Ehrenfest. Nei ferromagneti reali, la capacità termica diverge all'infinito.
Nel moderno schema di classificazione, le transizioni di fase sono divise in due categorie:
- Le transizioni di fase del primo ordine sono quelle che coinvolgono un calore latente. Durante tali transizioni, un sistema termodinamico assorbe o rilascia una quantità di energia fissa, e generalmente grande. Poiché l'energia non può essere istantaneamente trasferita dal sistema all'ambiente circostante, le transizioni del primo ordine sono associate a "regimi di fase mista" in cui alcune parti del sistema hanno completato la transizione, mentre altre ancora no. Questo fenomeno è familiare a chiunque abbia mai bollito un po' d'acqua: l'acqua non diventa subito vapore, ma forma una turbolenta mistura di acqua e vapore acqueo. I sistemi a fase mista sono difficili da studiare, a causa della loro dinamica violenta e difficili da controllare. Comunque, molte importanti transizioni sono incluse in questa categoria, comprese le transizioni solido/liquido/gas (aeriforme).
- La seconda classe è detta delle transizioni di fase continue, anche chiamate transizioni di fase del secondo ordine: queste non sono associate ad alcun calore latente. Esempi di transizioni di fase del secondo ordine sono la transizione ferromagnetica, la transizione superfluida e la condensazione di Bose-Einstein.
Diverse transizioni sono note come transizioni di fase di ordine infinito. Sono continue, ma non rompono alcuna simmetria. L'esempio più noto è la transizione di Berezinsky-Kosterlitz-Thouless nel modello XY in 2 dimensioni.
La maggior parte delle transizioni continue, e alcune di quelle del primo ordine, sono anche transizioni di fase quantistiche, responsabili, tra le altre cose, della separazione delle forze fondamentali, o del passaggio da un plasma di quark e gluoni, in cui questi ultimi sono liberi, alla materia adronica, dove invece sono confinati. Infine molte transizioni di fase quantistiche in gas elettronici in 2 dimensioni sono di ordine infinito.
[modifica] Proprietà delle transizioni di fase
[modifica] Punti critici
Nei sistemi contenenti fasi liquide e gassose, è presente una speciale combinazione di pressione e temperatura, nota come punto critico, dove la transizione liquido/gas diventa del secondo ordine. Vicino al punto critico, il fluido è sufficientemente caldo e compresso che la distinzione fra le due fasi è praticamente inesistente.
Ciò è associato al fenomeno dell'opalescenza critica: il liquido ha un aspetto simile al latte, dovuto alle fluttuazioni della densità a tutte le lunghezze d'onda possibili, incluse quelle della luce visibile.
[modifica] Simmetria
Le transizioni di fase spesso (ma non sempre) avvengono tra fasi a differente simmetria. Si consideri, ad esempio, la transizione tra un fluido (liquido o gas) e un cristallo. Un fluido, che è composto di atomi sistemati in modo disordinato ma omogeneo, possiede la simmetria traslazionale continua: ogni punto all'interno del fluido ha le stesse proprietà di qualsiasi altro punto. Un cristallo, d'altra parte, è formato da atomi sistemati in un reticolo regolare. Ogni punto nel solido non è simile agli altri, a meno che questi punti non siano separati da una stessa distanza reticolare.
Generalmente, in una transizione di fase, si può distinguere una fase più simmetrica rispetto alle altre. La transizione da una fase più simmetrica ad una meno simmetrica va sotto il nome di rottura di simmetria. Nella transizione fluido-solido, ad esempio, la simmetria rotta è la traslazione nel continuo.
La transizione ferromagnetica è un altro esempio di transizione con simmetria rotta, in questo caso l'inversione della corrente elettrica di spin e delle linee del campo magnetico. Questa simmetria è anche detta "simmetria su-giù" o di "inversione temporale". Si rompe nella fase ferromagnetica a causa della formazione di domini magnetici contenenti momenti magnetici allineati. All'interno di ogni dominio c'è un campo magnetico che punta in una determinata direzione scelta spontaneamente durante la transizione. Il nome "inversione temporale" deriva dal fatto che la direzione della corrente viene invertita quando sono invertite le coordinate temporali.
La presenza o meno di una rottura di simmetria è importante per la classificazione e quindi il comportamento della transizione di fase: è stato precisato da Landau che, dato un qualsiasi stato di un certo sistema, si può inequivocabilmente dire se sia o no in possesso di una particolare simmetria. Di conseguenza non è possibile deformare analiticamente una fase in un'altra in possesso di una simmetria differente: ciò significa che, ad esempio, è impossibile per la fase solido-liquido finire in un punto critico come il liquido-gas. Comunque, le transizioni con rottura di simmetria possono essere o di primo o di secondo ordine.
Tipicamente, la fase a più alta simmetria è sul lato più caldo della transizione, mentre quella a simmetria più bassa sul lato a temperatura più bassa. Questo è certamente il caso per le transizioni solido-fluido e ferromagnetica. Ciò accade perché l'hamiltoniana del sistema presenta tutte le simmetrie dello stesso, mentre a bassa energia alcune di queste mancano (questo fenomeno va sotto il nome di rottura spontanea di simmetria): a basse temperature, il sistema tende ad essere confinato in stati a bassa energia; alle temperature più alte, le fluttuazioni termiche consentono al sistema di accedere a stati ad energia maggiore e quindi alle altre simmetrie dell'hamiltoniana.
Quando la simmetria è rotta, è necessario introdurre una o più nuove variabili per descrivere lo stato del sistema. Ad esempio, nella fase ferromagnetica si deve introdurre la magnetizzazione, la cui direzione è scelta spontaneamente quando il sistema viene raffreddato al di sotto del punto di Curie. Tali variabili sono dette parametri d'ordine, poiché misurano il livello di ordine del sistema, e sono differenti a seconda del sistema che si sta studiando. Possono essere definiti anche per transizioni senza rottura di simmetria.
Le transizioni di fase con rottura di simmetria hanno un ruolo importante anche in cosmologia. Si è supposto che, nell'universo caldo delle origini, il vuoto possedesse un ampio numero di simmetrie. Con l'espansione e il raffreddamento dell'universo, il vuoto ha subito una serie di transizioni di fase con rottura di simmetria. Ad esempio la transizione elettro-debole ha rotto la simmetria SU(2)×U(1) del campo elettrodebole nella simmetria U(1) del ben noto campo elettromagnetico. Questa transizione è importante per comprendere l'asimmetria tra materia e antimateria presente nell'universo attuale.
[modifica] Esponenti critici e classi di universalità
Le transizioni di fase continue sono più facili da studiare di quelle del primo ordine a causa dell'assenza di calore latente, e si è scoperto che hanno diverse interessanti proprietà. Il fenomeno associato con le transizioni di fase continue è detto fenomeno critico, dovuto all'associazione con il punto critico.
Le grandezze termodinamiche delle transizioni di fase continue possono essere caratterizzate da parametri detti esponenti critici: all'avvicinarsi della temperatura T a quella critica TC, queste grandezze divergono secondo una legge di esponente a potenza. Utilizzando l'energia libera di Gibbs, si possono ricavare le espressioni di queste grandezze e quindi le dipendenze al limite. Ad esempio, per la suscettività magnetica si ha:
che, quando T ∼ TC, diverge secondo la legge:
Con il calore specifico si ottiene:
che segue la seguente legge di potenza:
La costante α è l'esponente critico associato con la capacità termica. Non è difficile vedere che deve essere inferiore a 1 per non avere calore latente durante la transizione. Il suo effettivo valore dipende dal tipo di transizione di fase considerata. Per -1 < α < 0, il calore specifico ha un "nodo" alla temperatura di transizione. Questo è il comportamento dell'elio liquido alla "transizione lambda" da uno stato normale a uno superfluido, per il quale gli esperimenti hanno trovato α = -0.013±0.003. Per 0 < α < 1, la capacità termica diverge alla temperatura di transizione (sebbene, per α < 1, la divergenza non è abbastanza forte da produrre un calore latente). Un esempio di tale comportamento è la transizione di fase ferromagnetica in 3 dimensioni. Nel modello di Ising in 3 dimensioni per magneti monoassiali, dettagliati studi teorici hanno calcolato l'esponente α ∼ 0.110.
Alcuni modelli non seguono questa legge di evoluzione. Ad esempio, la teoria di campo medio predice una discontinuità finita della capacità termica alla temperatura di transizione, mentre il modello di Ising in due dimensioni ha una divergenza logaritmica. Comunque questi sistemi sono un'eccezione alla regola: le transizioni di fase reali presentano leggi di potenza.
Si possono poi definire ben due esponenti critici legati al parametro d'ordine (che per comodità indicheremo con m):
m ∼ |T - TC|β
m ∼ h1 / δ
Per gli ultimi due esponenti critici che possono essere definiti - η e ν - bisogna, innanzitutto, introdurre la funzione di correlazione. La sua trasformata di Fourier, G(k), è legata all'esponente η dalla relazione:
dove ξ è la lunghezza di correlazione: è la lunghezza rilevante di scala, ovvero se due siti (o spin, nel caso ferromagnetico) sono a una distanza più grande di ξ, questi sono praticamente non correlati. Anche questa diverge secondo una legge di potenza:
ξ ∼ |T-TC|-ν
È importante il fatto che le transizioni di fase presenti in sistemi differenti posseggono lo stesso set di esponenti critici. Questo fenomeno è noto come universalità. Ad esempio, gli esponenti critici al punto critico liquido-gas sono risultati indipendenti dalla composizione chimica del fluido. Ancor più stupefacente: essi sono un'esatta stima per gli esponenti critici della transizione ferromagnetica nei magneti monoassiali. Tali sistemi sono detti classi di universalità. L'universalità è una predizione della teoria del gruppo di rinormalizzazione, che stabilisce che le proprietà termodinamiche di un sistema vicino alla transizione di fase dipendono solo da un piccolo numero di caratteristiche, come la dimensionalità e la simmetria, e che la transizione è insensibile alle proprietà microscopiche del sistema.
[modifica] Teoria di campo medio
Nel 1907, Pierre Weiss propose una teoria fenomenologica sul ferromagnetismo nella quale assunse che gli spin interagissero tra loro attraverso un campo molecolare proporzionale alla media (da qui teoria di campo medio) della magnetizzazione.
È quindi particolarmente interessante studiare una applicazione di tale teoria ad un sistema ferromagnetico. Per poterlo descrivere è utile introdurre un semplice modello reticolare, noto come modello di Ising.
[modifica] Modello di Ising
Il modello di Ising, costruito appositamente per un sistema ferromagnetico, cerca di rispondere a 2 precise richieste:
a) trovare equazioni abbastanza semplici da risolvere, possibilmente in maniera analitica, o al peggio con un computer;
b) non perdere in tale processo di semplificazione nessuna delle caratteristiche essenziali del sistema fisico che si vuole studiare.
La più semplice hamiltoniana che si può scrivere è:
dove i e j sono indici che identificano i siti del reticolo, J è una costante di accoppiamento positiva, mentre <i, j> indica che la somma va fatta sui primi vicini. Riguardo le due σ, se queste sono intese come matrici di Pauli, questa hamiltoniana definisce il modello quantistico di Heisenberg. Se con le σ si intendono, invece, i vettori di spin classici, allora si sta definendo il modello classico di Heisenberg. Si può ulteriormente semplificare, decidendo di prendere solo due valori possibili per σ = ± 1. Sarà proprio questa hamiltoniana con questi ultimi spin quella utilizzata nel modello di Ising.
A questo punto si può legare l'hamiltoniana con l'energia libera di Gibbs tramite la funzione di partizione, che lega l'hamiltoniana alla temperatura e consente di calcolare la probabilità di una particolare configurazione del sistema o il valore medio del campo (in questo caso la magnetizzazione):
Quest'ultima si lega molto semplicemente all'energia libera di Gibbs
[modifica] Approssimazione di campo medio
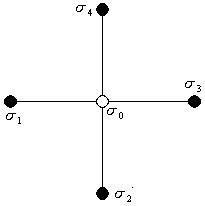
Risolvere il modello di Ising non è affatto semplice: è per questo che Weiss propose la sua approssimazione di campo medio. L'approssimazione si basa sulla seguente idea: si consideri un particolare spin σi, e si assuma che la corrispondente energia Ei possa essere calcolata sostituendo a tutti gli altri spin il loro valor medio <σi>. In questo modo ci si riduce ad un problema classico di paramagnetismo. È conveniente mettere, poi, il sistema sotto l'azione di un campo magnetico esterno h, che aggiunge artificialmente la rottura di simmetria sperimentata dal sistema; in questo modo l'hamiltoniana totale risulta avere la forma seguente:
dove μ σ = μ, momento magnetico.
Questa potrà essere legata all'energia libera tramite la funzione di partizione e da questa, attraverso la sua trasformata di Legendre, si potranno determinare gli esponenti critici:
Saranno infatti i minimi di quest'ultima a consentire il calcolo di tali esponenti, senza dimenticare che al posto di tutte le quantità con pedice i andrà sostituito il corrispondente valore medio, il tutto nel limite di h tendente a zero (il che significa ricordarsi che la transizione, in realtà, avviene senza alcun campo esterno).
L'approssimazione di campo medio, però, non è valida: la formulazione, poco sopra riassunta, pur risultando molto semplice, ha lo svantaggio di non considerare le fluttuazioni dei campi. Molte, allora, sono le teorie che cercano di ovviare a tale inconveniente per poter spiegare dati sperimentali altrimenti inspiegabili. Tra queste si può citare la teoria di Ginzburg-Landau, anch'essa una teoria di campo sul continuo.
[modifica] Transizione di fase del primo ordine in termodinamica
La transizione di fase in termodinamica è rappresentabile soddisfacentemente dal diagramma delle fasi: il diagramma delle fasi è un piano pressione e temperatura come quello indicato in figura. Per l'ambito termodinamico di base interessano solo le transizioni del primo ordine e nelle fasi comuni: solida, liquida e vapore.
Come si vede nelle figure ogni punto del piano (T,p) rappresenta un determinato valore dei parametri della sostanza (a volume costante, anche se non necessariamente). Ogni punto rappresenta quindi una ben determinata fase della sostanza, eccetto che i punti che si trovano sulle linee: queste linee curve vengono dette linee di transizione, che dividono nettamente le fasi della sostanza. Ebbene sulle linee di transizione avviene il passaggio da una fase all'altra della sostanza: la transizione avviene solo per determinate coppie di valori (T, p) e chiaramente dipendono dal tipo di sostanza. Il punto C è il punto critico, cioè il punto dato da (Tc,pc), che rappresenta il valore massimo della temperatura per il quale la sostanza si può trovare nello stato liquido, oltre tale temperatura la sostanza può trovarsi solo in stato gassoso.
Il punto Pt = (Tt,pt) è detto punto triplo: esso rappresenta l'unica coppia di valori per una determinata sostanza, nella quale le tre fasi coesistono simultaneamente. Questo punto è caratteristico per ogni sostanza e quindi viene usato con successo nella taratura della temperatura dei termometri.
Nelle due figure c'è una sottile ma importante differenza: la pendenza della curva di transizione liquido-solido. Nella figura 1 si ha l'andamento tipico delle transizioni per la maggior parte delle sostanze, come si vede l'aumento della pressione non provoca che piccole variazioni di volume in accordo con fatto che il liquido è poco comprimibile rispetto al solido. Viceversa la figura 2 mostra l'andamento caratteristico dell'acqua e di poche altre sostanze: la pendenza della curva è negativa ciò implica proprietà peculiari dell'acqua e delle sostanze che presentano tale diagramma. La più importante è il fatto che la densità dell'acqua liquida è maggiore di quella del ghiaccio, motivo per cui il ghiaccio galleggia sull'acqua.
L'equazione che caratterizza le transizioni di fase del primo ordine con pressione e temperatura che rimangono costanti, va ricercata nella conservazione del potenziale di Gibbs o energia libera di Gibbs: G = U + pV − TS = H − TS, dove U è l'energia interna, S l'entropia, H l'entalpia. Si arriva ad un'equazione detta Equazione di Clapeyron che può essere ricavata anche senza determinare i potenziali di cui sopra: il risultato è identico.
| Per approfondire, vedi la voce Equazione di Clapeyron. |
Consideriamo allora una trasformazione reversibile nella quale sono costanti la pressione e la temperatura: si conserva il potenziale di Gibbs:
ciò significa che per un cambiamento infinitesimo della pressione e temperatura, da 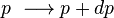 e
e  si avrà:
si avrà:
da cui:
dalla quale si ottiene l'equazione differenziale di Clapeyron:
dove λ rappresenta il calore latente di trasformazione.
Dobbiamo far notare che questa equazione non è risolubile immediatamente: vi è bisogno di certe accettabili approssimazioni, poiché λ dipende essa stessa dalla temperatura.
[modifica] Note
- ^ Quando si parla di "transizione di fase" si fa uso improprio del termine "fase", che in questo contesto indica lo stato di aggregazione (solido, liquido, gassoso).
- ^ Rolla, op. cit., p. 97
[modifica] Bibliografia
- Luigi Rolla, Chimica e mineralogia. Per le Scuole superiori, 29a ed. Dante Alighieri, 1987.
- (EN) H.Eugene Stanley, Introduction to Phase Transitions and Critical Phenomena, Oxford Science Publications (1971).
- (EN) Michel Le Bellac, Quantum and Statistical Field Theory, Oxford Science Publications (1991).
- (EN) Anderson, P.W., Basic Notions of Condensed Matter Physics, Perseus Publishing (1997).
- (EN) Goldenfeld, N., Lectures on Phase Transitions and the Renormalization Group, Perseus Publishing (1992).
- (EN) Landau, L.D. and Lifshitz, E.M., Statistical Physics Part 1, vol. 5 of Course of Theoretical Physics, Pargamon, 3rd Ed. (1994).
- Mussardo, G., Il Modello di Ising. Introduzione alla teoria dei campi e delle transizioni di fase, Bollati-Boringhieri, (2007).
[modifica] Voci correlate
[modifica] Altri progetti
 Wikimedia Commons contiene file multimediali su Transizione di fase
Wikimedia Commons contiene file multimediali su Transizione di fase
[modifica] Collegamenti esterni
| Maxwell Boltzmann | Bose-Einstein | Fermi-Dirac | |
|---|---|---|---|
| Aspetti generali |
Funzione di stato · Entropia · Temperatura |
||
| Insiemi statistici |
Insieme microcanonico · Insieme canonico · Insieme gran canonico |
||
| Particelle elementari | Particella classica | Bosone | Fermione |
| Distribuzioni statistiche | Statistica di Maxwell-Boltzmann | Statistica di Bose-Einstein | Statistica di Fermi-Dirac |
| Stati della materia | Gas ideale | ||